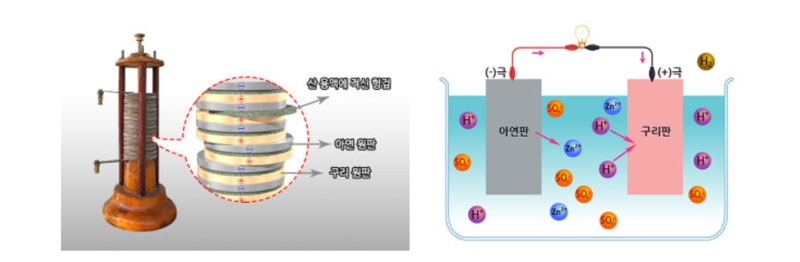
볼타전지
볼타전지(voltaic cell)는 자발적으로 일어나는 산화-환원 반응이 외부 회로(혹은 전선)로 연결된 전기화학 전지를 말한다. 갈바니 전지(Galvanic cell)라고도 한다. 볼타 전지의 명칭은 이탈리아 과학자인 알레산드로 볼타(Alessandro Volta)가 1800년 두 개의 다른 금속과 전해질로 만들어진 최초의 전지를 제작하여 화학 반응과 전기의 연관성을 발견하는 데 성공한 과학적 공로를 인정하여 그 이름을 따라서 붙인 전지 이름이다. 비록 볼타와 같은 이탈리아 출신의 갈바니가 두 종류의 서로 다른 금속으로 이루어진 해부용 칼이 개구리의 근육에 닿자 해부한 개구리의 근육이 움직인다는 사실을 관찰하여 전기가 화학과 관련되어 있다는 사실을 최초로 실험적으로 입증한 공로는 있으나, 오늘날 우리가 사용하는 전지의 실질적인 원형은 볼타가 발견한 것이다.[1]
개요[편집]
볼타전지는 묽은 황산을 전해액(電解液)으로 하여 그 속에 구리판(+극)과 아연판(-극)을 세우면, 약1.1V의 기전력(起電力)이 생긴다고 알고 있는 사람이 많으나 이는 잘못된 설명이다. 표준상태에서 아연의 환원 전위는 -0.76V이고 구리의 환원전위는 0.34V가 맞으나 실제 반응에서는 구리이온이 존재하지 않으므로 수소이온과 아연금속이 반응한다. 따라서 표준상태에서 0.00V-(-0.76V)=0.76V 의 기전력이 생긴다.
볼타전지의 발명은 전류의 지속적인 발생에 성공했다는 점에서 의의가 있으나, 대공업의 동력원으로서는 한계를 갖고 있다.[2]
화학전기의 발명[편집]
18세기는 초기의 전기현상 연구에서 많은 발견과 발명이 이어진 시기였다. 1745년에 무셴브뢰크가 라이든 병을 발명함으로써 정전기현상에 대한 연구가 활발해졌고, 18세기 중엽 프랭클린이 천둥을 전기방전현상으로 설명하였으며, 1780년대에는 쿨롱에 의해 쿨롱의 법칙이 증명되었다.
전지는 1780년에 처음으로 등장했다. 당시 해부학 교수였던 루이지 갈바니(1737~1798)는 해부한 개구리 다리가 금속제의 해부칼에 닿자 경련이 일어나는 것을 관찰했다. 갈바니는 이를 보고 전기가 개구리의 신경 속에 숨겨져 있다고 생각해서 '동물 전기'라고 이름을 붙였다. 하지만 이에 의문을 품은 알렉산드로 볼타(1745-1827)가, 전기는 종류가 다른 두 금속이 접촉하면 일어난다는 사실을 발견했다. 1799년에 금속 쌍을 산성 용액에 담그고, 잠기지 않은 두 끝을 연결하면 회로가 생겨 전기가 계속 흐르는 것을 발견하고, 그 원리를 이용해 최초의 화학전지를 발명했다.
볼타가 주장했듯이 전지에 있어서 주목해야 할 부분은 바로 서로 다른 두 종류의 금속의 접촉이다. 금속은 전자를 내놓고 양이온이 되는 성질을 가진 원소로서 이들이 전자를 내놓으려는 정도는 금속마다 다르다.
볼타가 만든 '전지'는 단발적인 전기 방전을 만드는 데 그치던 당시의 라이든 병과는 달리 전기가 계속적으로 흐르게 하는 장치였다. 그것은 당시 조금씩 생기고 있던 '전류'라는 개념으로 성큼 다가선 것이었다. 전지의 발명에 힘입어 19세기에는 전기에 관한 획기적인 과학적, 기술적 성과들이 쏟아져 나올 수 있었다.[3]
볼타 전지의 구성과 원리[편집]
볼타 전지의 구성[편집]
볼타는 수차례의 실험을 통해 두 종류의 서로 다른 금속과 습기만 있으면 전기가 발생된다는 것을 발견하였고, 인류 최초로 전류를 지속적으로 발생시킬 수 있는 볼타 전지를 발명하였다. 볼타 전지는 구리 원반과 산 용액에 적신 헝겊, 그리고 아연 원반을 교대로 쌓아서 만들어진 것이다.
- (-)극 : 양이온이 되기 쉬운 아연판 (아연이 황산 용액 속으로 녹아 들어간다.)
- (+)극 : 양이온이 되기 어려운 구리판(구리판 주위에서 수소 기체가 발생한다.)
- 전해질 용액으로 묽은 황산을 사용하여 아연판을 녹인다.
볼타 전지의 원리[편집]
볼타전지가 작동하는 원리는 금속들이 전자를 내놓으려는 정도가 다른 것을 이용한 것이다. 서로 다른 두 종류의 금속을, 전자가 이동하면서 반응을 일으킬 수 있는 용액과 접촉할 수 있는 상태에 두면, 화학 반응이 일어나 두 금속 사이에 전자의 흐름을 만들 수 있는 힘이 생기게 된다. 즉, 도선을 통해 반응성이 큰 금속에서 반응성이 작은 금속으로 전자가 이동하여 전류가 흐르게 된다.
아연판 (-)극 : 금속 아연은 수소보다 전자를 쉽게 잃고 녹아서 (+)이온으로 되어 황산 속으로 녹아들어간다.(황산 속의 H+ 보다 Zn이 이온화가 더 잘됨)
Zn → Zn2+ +2
구리판 (+)극 : H+이 구리판으로 이동해 간 전자를 받아서 H2로 되어 구리판에서 발생한다.
2H+ + 2 → 2H → H2↑
전체 반응 : Zn + 2H+ → Zn2+ + H2↑
분극 현상[편집]
볼타 전지를 이용하여 전구를 켜면, 켠 지 채 몇 분도 안 지나서 전구의 불이 꺼진다. 그것은 구리판 주위에 수소 기체가 생겨 전자의 흐름을 막기 때문에 생기는 현상으로, 이것을 '분극'이라고 한다. 과산화수소, 이산화망가니즈 등과 같은 산화제를 구리판 주위에 넣어 주면, 수소 기체가 물로 변하여 분극 현상이 없어지므로 전류가 잘 흐르게 된다. 이와 같은 현상을 '감극'이라고 하고, 이 때 쓰인 산화제를 '감극제(소극제)'라고 한다.[4]
각주[편집]
참고자료[편집]
- 〈배터리 상식-볼타전지, 다니엘 전지, 연료전지〉, 《네이버 지식백과》
- 〈볼타 전지〉, 《위키백과》
- 사이언스올, 〈1799년 볼타전지의 발명〉, 《사이언스타임즈》, 2004-10-28
- 운영자, 〈제목〉, 《홍익에스엠》, 2007-07-18
같이 보기[편집]
 해시넷
해시넷